Le Professeur Jean-Charles Deybach demande aux patients de connaître leur porphyrie. Ces pages essayeront de répondre à cette attente.
En introduction, vous allez découvrir la place de l’hème dans notre système sanguin.
Composants Sanguins
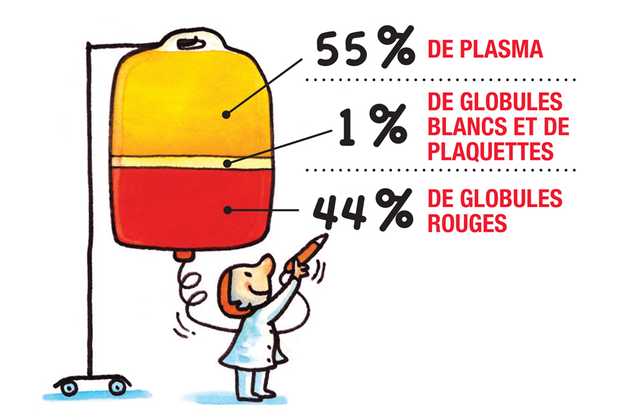
Le sang contient :
- du Plasma
Le plasma constitue 55 % du volume du sang total. Formé d’eau à 90 %, de sels, de lipides et d’hormones, le plasma est surtout un liquide riche en protéines, dont l’albumine, sa protéine principale; les immunoglobulines; ainsi que les facteurs de coagulation et le fibrinogène. Le plasma remplit plusieurs fonctions : le transport des cellules sanguines et des substances nutritives; la régulation de l’eau et des sels minéraux de l’organisme; l’irrigation des tissus; la défense contre les infections; la coagulation du sang. Les globules rouges, les globules blancs et les plaquettes se retrouvent en suspension dans le plasma.
- des Globules Blancs
On retrouve 6 000 à 8 000 globules blancs (ou leucocytes) par millimètre cube de sang. Un peu plus gros que les globules rouges, ils remplissent diverses fonctions de purification et de protection contre les infections. En effet, dès qu’une infection est présente dans un endroit du corps humain, les globules blancs s’y rendent pour la combattre.
- des Plaquettes
Les plaquettes (ou thrombocytes) sont des cellules sanguines plus petites que les globules. Elles ont pour fonction de contribuer à la coagulation sanguine et à la cicatrisation des plaies.
- des Globules Rouges
Une goutte de sang de la grosseur d’une tête d’épingle contient environ 5 millions de globules rouges (ou Hématies). Ce sont de petits disques biconcaves sans noyau dont la couleur rouge est due à une protéine appelée hémoglobine, une protéine contenant du fer. Chez les femmes, la masse des globules rouges occupe de 37 à 43 % du volume sanguin; chez l’homme, de 43 à 49 %. Les globules rouges ont pour fonction le transport de l’oxygène.
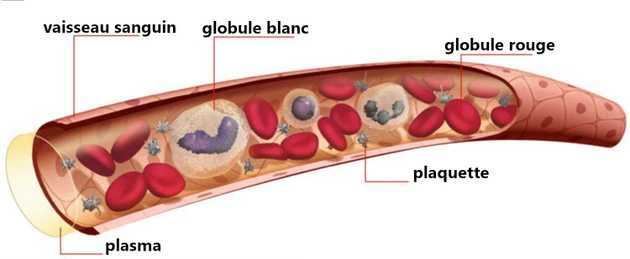 Illustration tirée du Nouveau Dictionnaire Visuel, www.quebec-amerique.com, éditions Québec Amérique inc.
Illustration tirée du Nouveau Dictionnaire Visuel, www.quebec-amerique.com, éditions Québec Amérique inc.
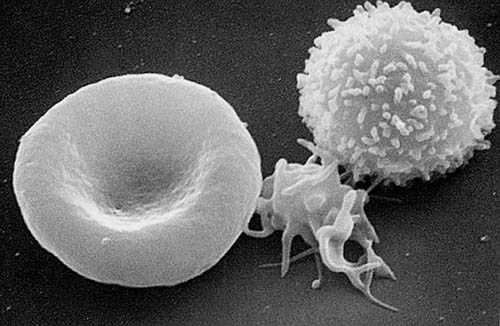 De gauche à droite : un globule rouge, une plaquette sanguine, un globule blanc. Source : Wikipedia
De gauche à droite : un globule rouge, une plaquette sanguine, un globule blanc. Source : Wikipedia
Pour nous les globules rouges sont importants, car ils contiennent l’hème.
Globules Rouges
La composition des globules rouges explique la différence de couleur de sang chez les vertébrés et chez les invertébrés. En effet, ces cellules sont constituées d’hémoglobine chez les vertébrés et d’hémocyanine chez les invertébrés.
Rouge chez les vertébrés
L’hémoglobine contient différents atomes : du carbone, de l’azote et du fer.
Les globules rouges transportent le dioxygène vers nos différents organes. Pour faire cela, le dioxygène va se fixer sur les atomes de fer de l’hémoglobine. Or, le fer associé au dioxygène créé une nouvelle molécule qui est de couleur rouge. Ce phénomène est appelé oxydation du fer, et c’est la raison pour laquelle notre sang est de couleur rouge.
Histoire de faire des comparaisons, c’est également à cause de l’oxydation du fer que se forme la rouille qui est de couleur rouge.
 La rouille. Source : Science Junior
La rouille. Source : Science Junior
Transportées par les globules rouges dans la circulation sanguine, les molécules d’hémoglobine assurent l’apport du dioxygène aux différents organes des animaux vertébrés.
Le circuit du fer dans l’organisme humain
Le fer possède une circulation dans l’organisme, on n’excrète pas de fer dans les urines, le fer est absorbé et conservé.
- L’intestin va l’absorber.
- Le foie va le stocker et servir de tour de contrôle pour son métabolisme.
- La moelle osseuse est le site utilisateur majeur à cause de l’hème pour les globules rouges, c’est elle qui a besoin de fer en majorité.
Le recyclage: les globules rouges ont une durée de vie limitée à 120 jours, ils sont dégradés par les macrophages, l’hème est également dégradé.
L’hème essentielle à l’oxygénation des cellules de notre corps
Grâce au circuit du Fer nous avons vu que c’est l’hème, contenant du fer, qui permet de transporter le dioxygène (O2) dans notre corps.
 Illustration de www.docteurclic.com
Illustration de www.docteurclic.com
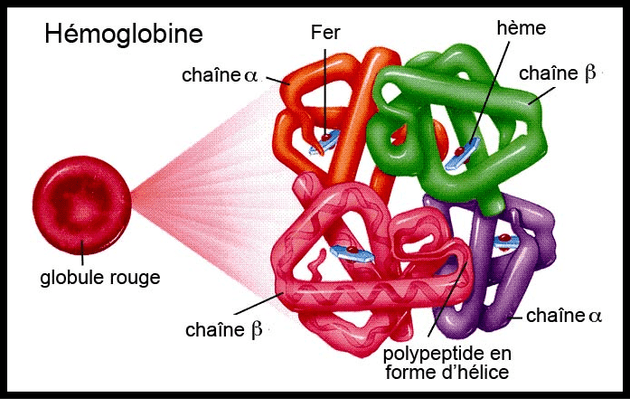
L’hémoglobine est un assemblage de quatre sous-unités qui abritent chacune une structure chimique particulière nommée “hème”. Chaque hème contient un ion ferreux Fe2+. Cet ion Fe2+ est responsable de la fixation d’une molécule de dioxygène (O2).
L’hème étant liée à la protéine d’hémoglobine et contenant un atome de fer sous forme ferreux Fe2+ en son centre peut fixer les molécules de dioxygène (O2) afin de permettre à la molécule d’hémoglobine de transporter l’oxygène dans le sang puis dans les tissus où la pression partielle en oxygène sera basse.
Les molécules de la Vie
Dans l’Antiquité, les Grecs récoltaient des coquillages de la famille des murex, dont ils extrayaient un pigment de couleur pourpre qu’ils utilisaient pour teindre les tissus. Aujourd’hui, le terme grec porphureos, qui signifie pourpre, a donné son nom à la classe de pigments la plus abondante dans la nature, les porphyrines. Produites tant chez les animaux que chez les végétaux, et même chez certaines bactéries, ces molécules en forme d’anneau entrent dans la composition d’éléments essentiels à la vie.
Liées à un ion magnésium, les porphyrines végétales forment la chlorophylle, indispensable à la photosynthèse. Combinées à un ion fer, les porphyrines animales forment l’hème, un motif nécessaire à la fonction de nombreuses métalloprotéines : l’hème de l’hémoglobine des globules rouges assure le transport de l’oxygène et du dioxyde de carbone dans le sang, et c’est encore l’hème d’autres protéines qui soutient les chaînes de transport d’électrons dans la respiration cellulaire (la production d’énergie dans les cellules) ou qui contribue aux activités catalytiques de nombreuses enzymes. Associées au nickel, les porphyrines forment la coenzyme F430, qui joue un rôle majeur chez les bactéries métabolisant le méthane. Enfin, la vitamine B12, produite par des micro-organismes (bactéries, champignons, algues), résulte de la combinaison du cobalt avec un dérivé des porphyrines.
Toutes ces molécules issues des porphyrines, nommées métalloporphyrines, sont construites sur le même schéma : un anneau – la porphyrine – au sein duquel est niché un ion métallique. Chacune est un pigment : elle absorbe la lumière visible, ce qui donne une couleur aux cellules qui en contiennent (vert pour la chlorophylle, rouge pour l’hémoglobine, jaune pour la coenzyme F430, rouge pourpre pour la vitamine B12). De par leur rôle clé chez presque tous les organismes vivants, on les surnomme parfois les couleurs de la vie.
 Représentation d’un globule rouge transportant du dioxygène dans le dessin animé “La vie”
Représentation d’un globule rouge transportant du dioxygène dans le dessin animé “La vie”
Leur universalité en fait l’objet de nombreuses recherches dans des domaines aussi variés que la médecine, l’agriculture ou les énergies renouvelables. Chez l’homme, des anomalies dans la synthèse des porphyrines entraînent de graves pathologies, les porphyries. Leur étude vise à mieux diagnostiquer et traiter ces maladies génétiques. Chez les végétaux, les agronomes ont développé des herbicides qui tuent les plantes nuisibles en perturbant la synthèse des porphyrines. D’autres travaux utilisant les propriétés photoniques des porphyrines ont pour objectif la mise au point de photothérapies ou de cellules photovoltaïques.
Fabrication ou Biosynthèse de l’hème
Cette molécule importante pour la vie qui est rouge chez l’homme en raison de l’atome du Fer, comment est-elle fabriquée ?
La fabrication s’effectue principalement sur deux sites. 80% de l’hème est produit par la moelle osseuse pour fabriquer les globules rouges (Erythropoïèse : chaque jour 200 milliards de globules rouges sont produits par la moelle osseuse de l’adulte sain) et 15% par le foie en fonction des besoins et le reste par le rein (négligeable).
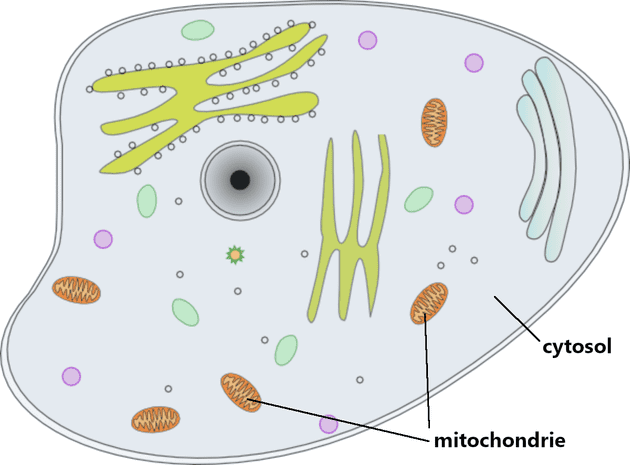 Cellule de la moelle osseuse ou du foie ou du rein.
Cellule de la moelle osseuse ou du foie ou du rein.
Au niveau cellulaire, la fabrication de l’hème va intervenir dans ces deux endroits :
- la Mitochondrie : une mitochondrie est un organite entourée d’une double membrane, elles sont localisées préférentiellement au niveau des zones cellulaires consommatrices d’ATP (l’ATP fournit l’énergie nécessaire aux réactions chimiques du métabolisme). Sa fonction est de participer à la chaîne respiratoire de l’organisme et de fournir de l’énergie pour de nombreuses réactions chimiques.
- et le Cytosol ou Cytosole : la phase liquide dans laquelle baignent les organites cytoplasmiques, présents à l’intérieur des cellules est appelée le cytosole. Elles est composée aussi d’ions inorganiques en grande quantité, de gaz dissous, de glucides, de lipides, d’acides aminés, de nucléotides, de métabolites divers, de protéines, etc.
Cette fabrication ou bien cette biosynthèse débute dans la mitochondrie (première étape : 1), se poursuit dans le cytosol (étapes : 2, 3, 4 et 5) et s’achève dans la mitochondrie (3 dernières étapes : 6, 7 et 8).
Biosynthèse de l’hème et Porphyries
Les porphyries sont un groupe de défauts de synthèse de l’hème débouchant sur l’accumulation de certains de ses précurseurs (les huit enzymes) et sur des symptômes cliniques caractéristiques. Le tableau ci-dessous montre les huit enzymes qui interviennent lors de la biosynthèse de l’hème et la Porphyrie correspondante s’il y a une défaillance lors de la production de l’hème.
| Enzyme | Porphyrie | Fréquence |
|---|---|---|
| 1 ALA-synthase | - | - |
| 2 PBG-synthase (ALA déhydratase) | Déficience en PBG-synthase | Inconnue |
| 3 PBG-déaminase | Porphyrie intermittente aiguë | 1-2 / 100 000 |
| 4 Uroporphyrinogène III synthase | Porphyrie érythropoiétique congénitale | < 1 / 1 000 000 |
| 5 Uroporphyrinogène décarboxylase | Porphyrie cutanée tardive | 1 / 25 000 |
| 6 Coproporphyrinogène oxydase | Coproporphyrie héréditaire | 1 / 250 000 |
| 7 Protoporphyrinogène oxydase | Porphyrie variegata | 1 / 250 000 |
| 8 Ferrochélatase | Protoporphyrie érythropoiétique | 1 / 200 000 |
-
D’un point de vue clinique, on distingue deux types de manifestations (apparaissant ensemble ou séparément):
- 1 - crises aiguës (signes abdominaux et neurologiques)
- 2 - atteintes cutanées (fragilité et photosensibilité)
Pour aller plus loin
- Voici pour les plus savants voici un topo scientifique:
La synthèse de l’hème a lieu principalement dans la moelle osseuse (85%) et le foie. Au niveau cellulaire interviennent au moins 8 enzymes différentes, ayant des localisations cytoplasmique et mitochondriale. L’enzyme limitante est l’ALA-synthase. Elle subit le feed-back négatif de l’hème, produit final du cycle, qui agit au niveau post-traductionnel, en bloquant la translocation de la pro-ALA-synthase dans la mitochondrie et au niveau de la synthèse de l’enzyme, en diminuant la stabilité de son ARNm. La PBG-déaminase pourrait être une seconde enzyme limitante, particulièrement au niveau hépatique.
Porphyrines
Les intermédiaires de la biosynthèse de l’hème sont les porphyrinogènes. Dans les liquides biologiques, particulièrement en milieu acide, ils s’oxydent spontanément en porphyrines. En pratique, ce seront donc les porphyrines que l’on recherchera.
Les porphyrines sont des dérivés de la porphine, une molécule macrocyclique hautement insaturée et composée de quatre noyaux pyrroles reliés par des ponts méthène. Il existe une multitude de porphyrines dans la nature, dont 3 types sont cliniquement intéressants: les uroporphyrine, coproporphyrine et protoporphyrine.
Les propriétés physico-chimiques de ces substances jouent un rôle important dans la pathogenèse des porphyries:
la conjugaison des doubles liaisons de ces molécules leur confère, au contraire des porphyrinogènes, des propriétés de coloration (absorbance maximale vers 405 nm - bande de Soret) et de fluorescence (vers 620 nm pour une excitation à 400 nm);
la substitution variable des noyaux pyrroles par des groupes carboxyls va déterminer leur solubilité. Les porphyrines, déposées dans la peau qui est ensuite exposée à la lumière ultraviolette, vont causer des dégâts tissulaires considérables. Les uro et coproporphyrines, hydrosolubles, se distribuent dans les liquides intra et extracellulaires et provoquent des lésions bulleuses retardées alors que la protoporphyrine, liposoluble, s’accumule plutôt au niveau membranaire et provoque une réaction inflammatoire avec sensation de brûlure quasi immédiatement après exposition au soleil.
La solubilité des porphyrines explique aussi les profils d’excrétion. Ainsi, l’uroporphyrine (octacarboxylique) est hydrosoluble au pH physiologique et se retrouvera surtout dans les urines. La protoporphyrine (dicarboxylique) est liposoluble et est excrétée essentiellement dans les selles. La coproporphyrine (tétracarboxylique) présente une solubilité intermédiaire et est éliminée par les 2 voies.
Les précurseurs des porphyrines (ALA et PBG) sont librement excrétés par le rein, ce qui explique leurs taux sanguins toujours très bas. Ils pourraient avoir un rôle direct dans la pathogenèse des signes neurologiques.